關於COVID-19新冠疫苗的誤解與迷思
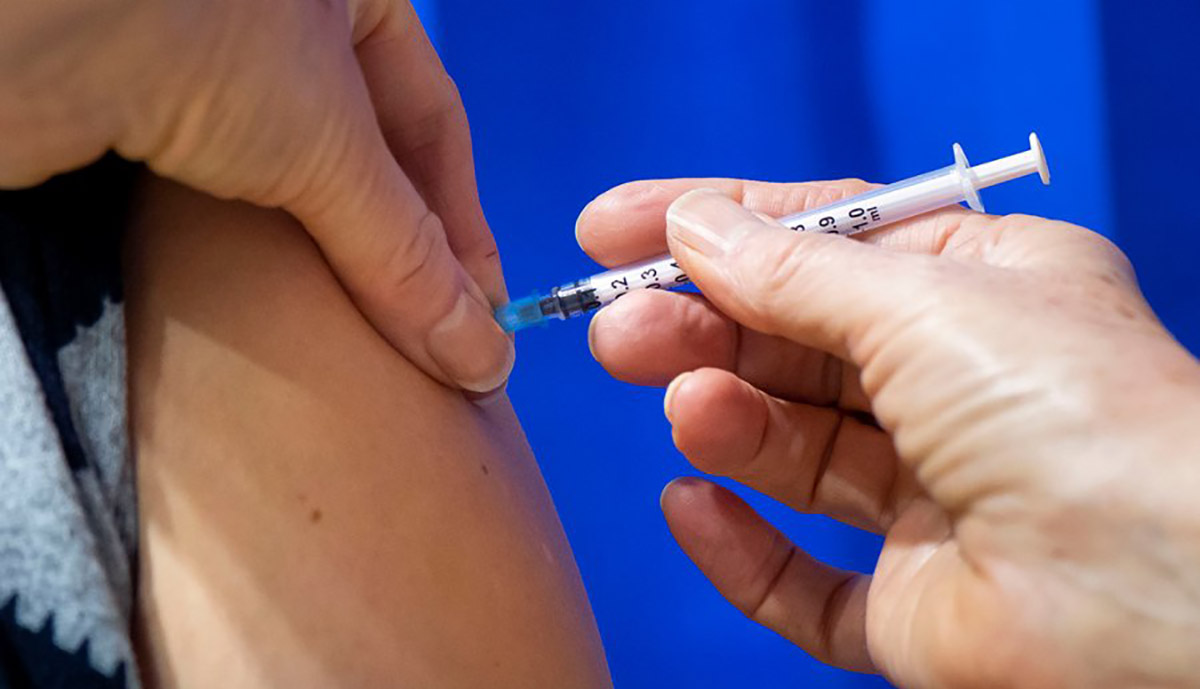
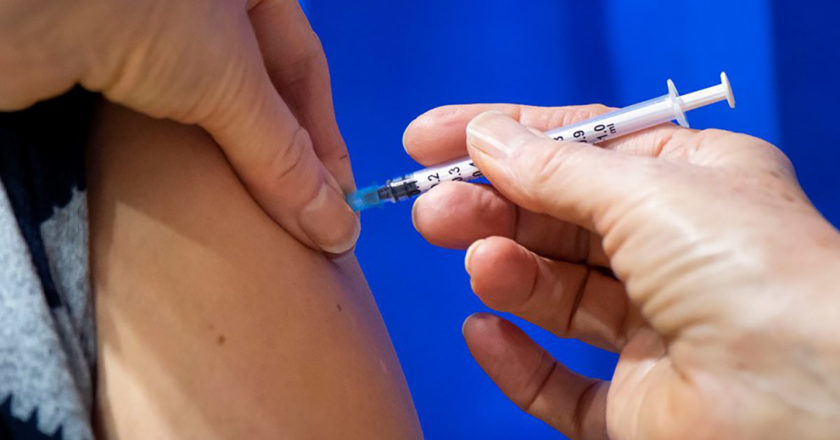
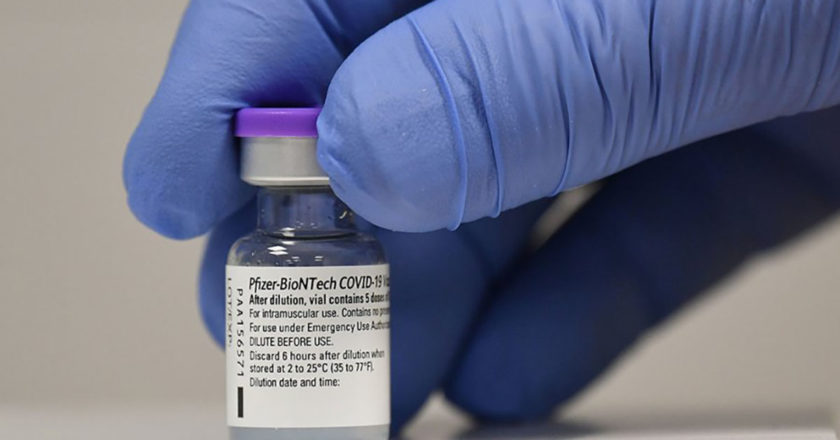
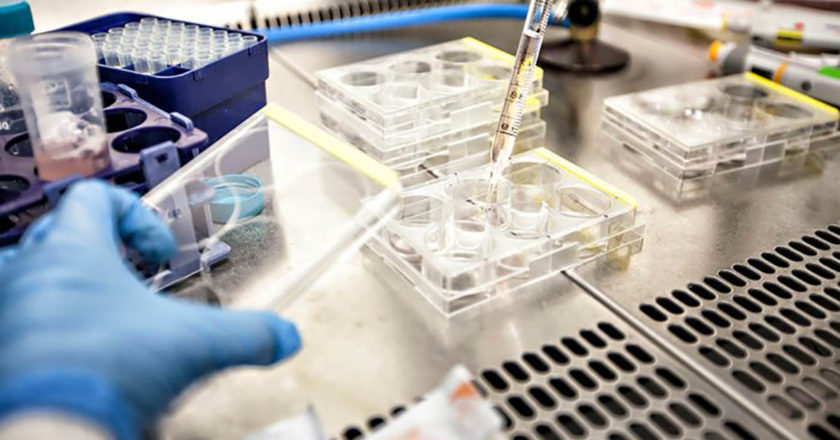
聯邦政府已經授權了第一款來自輝瑞的 COVID-19 疫苗(第二款Moderna疫苗也已經向FDA提交了緊急使用授權,預計有望在本週獲得批准),以此來減緩新冠病毒的傳播,並幫助結束疫情。
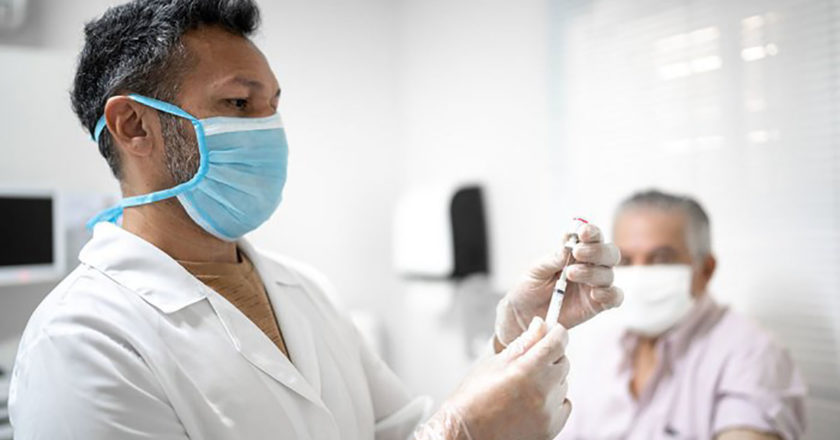
但是,疫苗的研發速度之快史無前例,造成了很多誤解,也讓一些美國人抱持懷疑。以下是對新冠疫苗的普遍誤解,以及 COVID-19 治療藥物的真實情況。
誤解 1:如果曾經患過 COVID-19,則無需接種疫苗。
如果之前感染過 COVID-19,將會得到多久的保護免受 COVID-19 感染(即自然免疫力),對於這一點還沒有定論。實際上,疾病預防與控制中心 (Centers for Disease Control and Prevention, CDC) 說明:「早期證據顯示從 COVID-19 獲得的自然免疫力可能不會持續太長時間。」因此,該機構表示:「即使是曾經患過 COVID-19 的人,也建議接種 COVID-19 疫苗。」
衛生官員瞭解更多有關自然免疫力持續時長的情況後,會隨時將任何進展和建議告知公眾。
誤解 2:接種新冠疫苗後,就會終身免疫。
新冠疫苗提供的免疫力能持續多長時間,以及是否需要多次接種,或像流感疫苗一樣需要定期接種,對於這些事項也尚不知曉。
國家衛生研究院 (National Institutes of Health, NIH) 主任兼醫學博士 Francis Collins 在最近的 AARP 樂齡會遠距全員大會上談到這個問題:「目前我們應該把這種疫苗看作是和破傷風疫苗相同的類型,而破傷風疫苗需要每隔幾年就接種一次。」他補充道:「如果我們足夠幸運,就會像麻疹一樣,只要免疫,就會終身免疫,但那得非常幸運。」
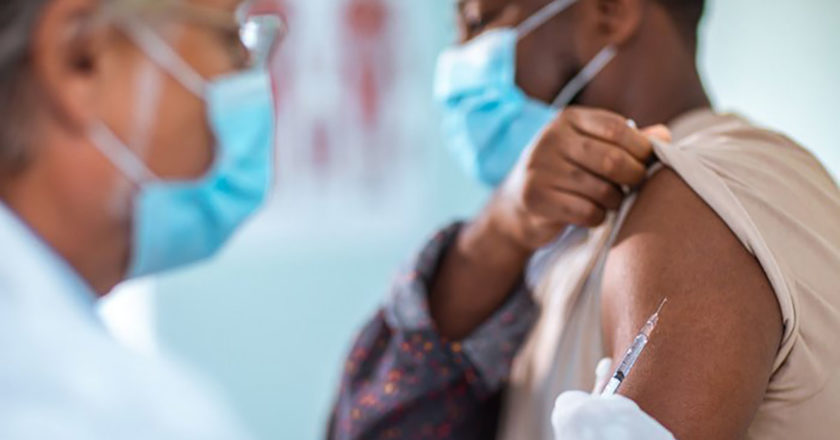
誤解 3:接種疫苗後就不用戴口罩了。
疫苗是幫助減少冠狀病毒傳播的一個工具,但還需要採取其他措施才能結束疫情,包括佩戴口罩、保持社交距離、經常洗手以及進行檢測。
其中一個原因是:衛生官員預測,可能需要幾個月的時間才能讓大部份想接種新冠疫苗的美國人完成接種。在相當比例的人口產生 COVID-19 抗體之前,也就是達到所謂的群體免疫之前,病毒會繼續傳播並使人患病。
另外一個原因是:保護並不會即時產生。CDC 解釋,身體在接種疫苗後「通常需要幾週」才能產生針對這種病毒的記憶細胞。這表示當一個人剛接種疫苗後「也可能會感染冠狀病毒」並罹患 COVID-19,「因為沒有足夠的時間讓疫苗產生保護作用」。
誤解 4:mRNA 疫苗可能改變人的 DNA。
在美國的後期試驗中,四種候選疫苗中的兩種(Pfizer/BioNTech 疫苗和 Moderna/NIH 疫苗)採用了一種稱為訊息 RNA(簡稱 mRNA)的新技術。可以將 mRNA 看作是一本指導手冊:它指導身體對某種特定感染產生免疫反應。
目前,美國沒有獲得許可的 mRNA 疫苗,它們的新穎性引起了人們的懷疑。社交媒體上流傳甚廣的一種說法稱,mRNA 疫苗能改變人類 DNA。CDC 專家表示,事實並非如此。
誤解 5:對於兩劑疫苗,不需要接種兩次。
在開發的後期階段,除一種疫苗外,所有疫苗都需要接種兩次,兩劑疫苗相隔幾週。因為健康專家不確定一劑疫苗是否足以有效預防 COVID-19 或重症情況,因此不進行第二次接種不是好主意。
約翰霍普金斯大學彭博公共衛生學院國際疫苗獲取中心執行主任兼醫學博士 William Moss 在此前的一次採訪中告訴 AARP 樂齡會:「我們不知道如果只接種一劑會出現什麽情況。」他補充道:「當然,我們不能期望 [一劑疫苗能提供] 高效的保護 ,[達到第三期臨床試驗中兩劑疫苗所產生的效果]。」
誤解 6:如果今年接種了流感疫苗,則無需接種新冠疫苗。
雖然流感和 COVID-19 都有一些相同的症狀,但這是兩種不同的疾病,由兩種不同的病毒引起。國家過敏和傳染病研究所 (National Institutes of Allergy and Infectious Diseases, NIAID) 主任兼醫學博士 Anthony Fauci 在近期 AARP 樂齡會遠端全員大會中稱,談到疫苗時「並不是二選一的問題」。
Fauci 表示:「你會需要得到針對流感和新冠病毒的雙重保護。」特別是因為兩種病毒有可能同時感染或接續著感染,對肺和其他器官造成負擔。
如果您對於AARP樂齡會有任何問題,歡迎撥打中文熱線1-888-832-1888諮詢。
了解更多關於新型冠狀病毒COVID-19的資訊,請瀏覽AARP樂齡會中文官網專頁https://chinese.aarp.org/covid-19/或掃描下方二維碼,關注AARP樂齡會官方微信公眾號。
點擊閱讀更多關於新冠疫苗的資訊:
#疫苗 #新冠疫苗 #輝瑞 #Pfizer #Moderna #誤解 #謠言 #AARP # AARP樂齡會 #求助熱線
本文原作者:Rachel Nania
原文鏈接:https://www.aarp.org/health/drugs-supplements/info-2020/covid-vaccine-myths.html
本文內容由AARP樂齡會原創,版權所有。未經同意不得轉載。