FDA 批准為免疫功能低下患者施打 COVID 疫苗增強劑
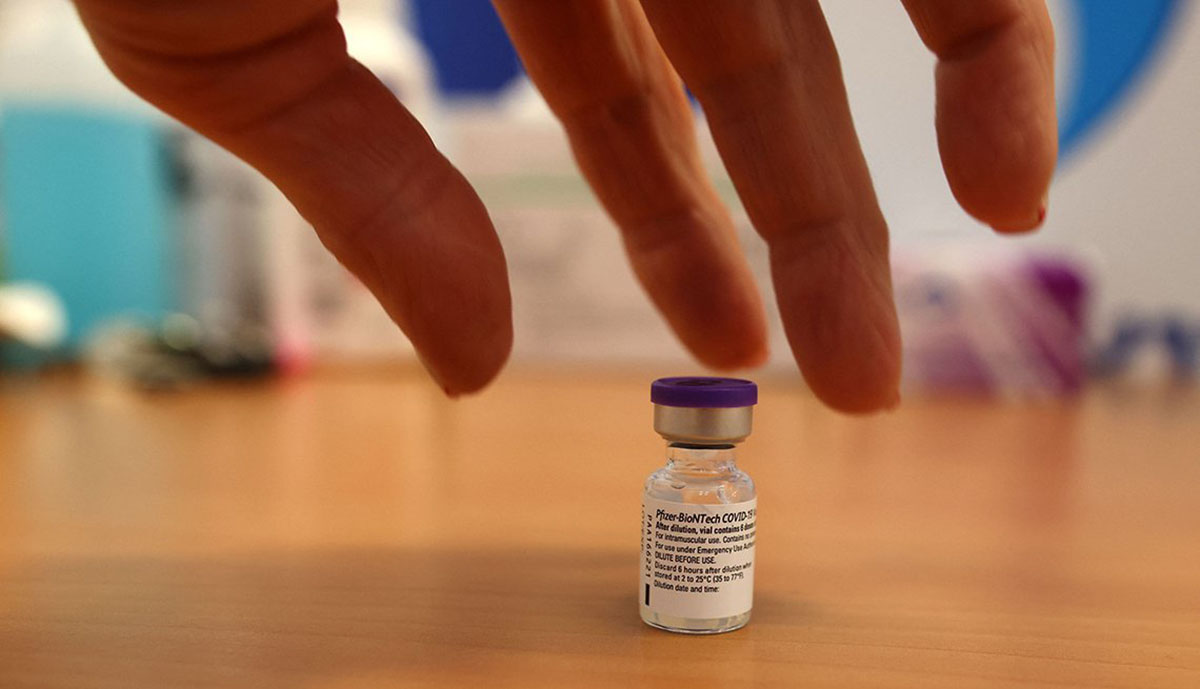
食品藥品監督管理局 (Food and Drug Administration, FDA) 於 8 月 12 日星期四擴大了 Pfizer-BioNTech 和 Moderna 疫苗的緊急使用授權 (EUA),允許免疫系統受損的人群接受第三劑「增強」劑,因為 COVID-19 病例、住院率和死亡率繼續在美國攀升。
根據疾病控制與預防中心 (Centers for Disease Control and Prevention, CDC) 主任 Rochelle Walensky 的說法,此次修正影響了不到 3% 美國成年人的少數人群,他們的免疫系統由於實體器官移植或者其他對免疫系統有同樣致殘作用的病症而弱化。
FDA 代理局長 Janet Woodcock 在一份聲明中稱:「在對可用的資料進行詳盡審查後,FDA 確定了該小規模的脆弱群體可能受益於 Pfizer-BioNTech 或 Moderna 疫苗的第三劑。今天的動作幫助醫生為某些需要更多 COVID-19 保護的免疫功能低下患者增強免疫力。」
FDA 解釋說,經歷過實體器官移植或有其他減弱免疫力病症的人,對抗感染的能力會下降,更有可能因感染生病。但是,施打第三劑疫苗可以向免疫系統注入抵抗 COVID-19 所需的力量,這一點尤其值得關注,因為具有高度感染性的 delta 變種正在肆虐全國的許多社區。
一項本週在 The New England Journal of Medicine 發表的研究發現,與接受安慰劑增強劑的患者相比,接受了第三劑疫苗的實體器官移植患者對新冠病毒產生了顯著的抗體反應增強。該研究的研究人員寫到,接受第三劑的患者的一些副作用要比接受安慰劑組稍微更普遍,但在施打第三劑後未報告嚴重的不良事件。
CDC 專家將權衡額外劑量
在可以施打增強劑之前還有一步。
CDC 召集的諮詢委員會於 8 月 13 日星期五正討論 FDA 擴大 Pfizer 和 Moderna EUA 的決定。該小組將投票表决是否建議增強劑,並且將進一步明確誰應該施打、將怎樣施打。
在 Walensky 的批准之後,最快可能在本週末提供增強劑。
Walensky 在星期四的新聞發布會上說:「此動作是為了確保我們最脆弱,可能需要額外劑量以增強對疫苗生物反應的人群能得到防禦 COVID-19 的更好保護。」
修正的 EUA 允許在接種兩劑同一疫苗後的至少 28 天施打第三劑,Moderna 允許的對象是 18 歲或以上的人群,Pfizer-BioNTech 允許的是 12 歲或以上人群。至於接種了單劑 Johnson & Johnson 疫苗的人,並未提及增強劑。
其他人還不需要增強劑
在 FDA 宣布 EUA 擴大的新聞發布會上,Woodcock 重申:「已完全接種疫苗的其他人得到了充分的保護,目前不需要 COVID-19 疫苗的額外劑量。」但是,專家稱,其餘人群接種 COVID-19 增強劑很可能是無法避免的。現在只是不清楚將何時需要,或者誰將是下一批需要接種的。
國家過敏和傳染病研究所 (National Institute of Allergy and Infectious Diseases) 主任 Anthony Fauci 在星期四的新聞發布會上說:「我們認為,非免疫功能低下的其他人,無論是年長者還是非年長者,目前不需要增強劑。但這是一個動態的過程,我們將評估資料。」
當做出決定,向更多人群開放增強劑後,Fauci 說官員們「已做好準備,並且能迅速動作」。白宮新冠病毒應對協調員 Jeffrey Zients 強調,全國有充足的供應量,「民眾將能快速、高效地接種增強劑」。
如果您對於AARP樂齡會有任何問題,歡迎撥打中文熱線1-888-832-1888諮詢。
了解更多關於新型冠狀病毒COVID-19的資訊,請瀏覽AARP樂齡會中文官網專頁https://chinese.aarp.org/covid-19/或掃描下方二維碼,關注AARP樂齡會官方微信公眾號。
點擊閱讀更多關於COVID-19疫苗的資訊:
本文原作者:Rachel Nania
本文內容由AARP樂齡會原創,版權所有。未經同意不得轉載。

